Ennov regulatory suite
Dossier
申請書類パブリッシング
ソフトウェア
- 薬機申請書の作成、管理、提出
- 任意の出力形式で提出する
- 強固なハイパーリンクとブックマーク
- 内蔵されたバリデーション機能により、規格に準拠した提出が可能
- 100% Webベース、グローバル展開に最適
申請書類の課題
薬機法に準拠した申請書類を効率的に作成することが、すべての規制業務の目標です。多様な申請書の出力フォーマットを効果的に作成できる単一のパブリッシング・ソリューションがあれば、柔軟性、トレーニング、および総所有コストの面で明らかな利点が得られます。
Ennov Dossierは、あらゆる規模の規制業務に適した、包括的で拡張可能な書類管理および申請書類パブリッシング・ソリューションです。Ennov Dossierは、現在の医療関係機関のすべての要件に準拠したアウトプットを生成します。
- 刊行物用のCTD (国際共通化資料)
- 電子出版物用のeCTD及びNeeS (eCTD以外の電子申請)
- 獣医分野用のvNeeS
医療機器向けeCopy
Ennov Dossierは包括的で、直感的で使いやすく、薬機法規制機関への提出に関する最も厳しい要件を満たしています。
効率的で使いやすい
Ennov Dossierは、Ennov Docのネイティブ機能を使用して、規制関係書類を作成、管理、発行、検証、アーカイブする機能を提供します。
これにより、薬機法規制機関への提出に必要な文書の検索、コピー、アップロードという断片的で非効率的なプロセスが排除され、シームレスな統一された文書パブリッシング・ソリューションが提供されます。
シンプルなドラッグ&ドロップ・インターフェイスにより、発行者は文書を迅速かつ容易に申請アセンブリにリンクできます。
統合EDMSによる生産性の向上
Ennov Dossierは、Ennov Docと組み合わせることで、弊社の包括的なEDMSのすべての強力な機能を使用して薬機関係書類を管理する機能を提供します。
関係書類のライフサイクル、ワークフロー、通知を自動化することで、細分化された手作業が排除され、生産性が向上します。
Ennov独自のメタデータベースのナビゲーションは、ファイル階層内の保管場所ではなく、プロパティを使用して書類をすばやく見つけることができるため、生産性の向上にも役立ちます。
毎回薬機法に準拠した申請書類
申請アセンブリテンプレートは、eCTD申請を受け付ける地域 (米国、EU、GCC、カナダ、Swissmedic、TGAなど) およびその他のeCTD以外の形式で提供されており、お客様の個別の要件に合わせて変更できます。Ennovは、薬機法ガイダンスの変更に応じて、これらのテンプレートを定期的に更新します。
Ennov Dossierには、目次、ハイパーリンク、ブックマーク、その他のナビゲーションサポート機能もあり、申請書類のレビューに役立ちます。
必要なICHおよび各国のXMLファイルを含め、準拠する申請に必要なすべてのコンポーネントを発行する際に、適切な名前のリーフファイルとフォルダ構造が作成される。
中核的な機能
- CTD、eCTD、NeeS、VNeeS、eCopyに対応
- 関係書類のライフサイクル管理
- eCTDシーケンスおよびメタデータの管理
- 強固なハイパーリンクとブックマーク
- 統合されたeCTDバリデーション機能
- 提出書類のテンプレートを搭載
- 全文検索とメタデータベース検索
主な特長
- Ennov Docと本質的に連携
- 直感的なドラッグ&ドロップ式のユーザーインターフェース
- WebDAVに準拠したあらゆるリポジトリに対応
- コンプライアンスに準拠したPDFの自動レンダリング
- 100% Webベース
Aguettantのケーススタディ
薬事規制システムマネージャ Cyrille JEUNE
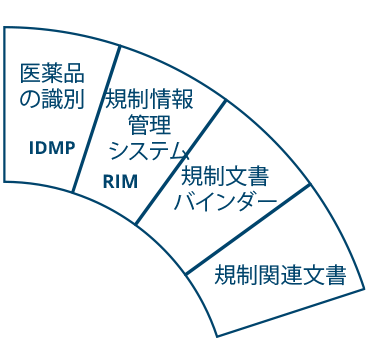
Ennov Regulatory
世界最高水準の規制コンテンツと情報管理
Ennov Regulatory Suite は Ennov Doc、Ennov Dossier、Ennov Process の機能と柔軟性を組み合わせ、登録目標の初期計画から製品の廃止まで、規制当局の製品ライフサイクル全体にわたってサポートするものです。Ennov Regulatory Suiteは、規制当局の活動計画、製品登録管理、資料作成、資料管理などにおいて非常に有用なツールです。
Ennovを選ぶ理由
Ennovを信頼する数百社の顧客企業
20年以上にわたるライフサイエンス分野におけるソフトウェアソリューションの提供経験
ライフサイエンス分野の顧客は250社以上、その他の業界も多数
最新のアーキテクチャとインタフェース
WEBベース100%. 高い拡張性. ユーザー重視の設計
お客様の成功のために
顧客満足度が非常に高く、98.5%のプロジェクトが期限内、予算内に納品されている
お客様の選択の自由を尊重
クラウドベースまたはオンプレミスでの導入が可能
配置オプションの切り替えはいつでも可能
お客様の自主性を尊重
システム構成および管理に関するITスキルは不要
セキュリティの向上とパフォーマンスの最適化
データはローカルに保存されるが、柔軟性に富む。シングルテナントであるため、業務の中断を最小限に抑えられる

クラウドベースまたはオンプレミス

マルチプラットフォーム