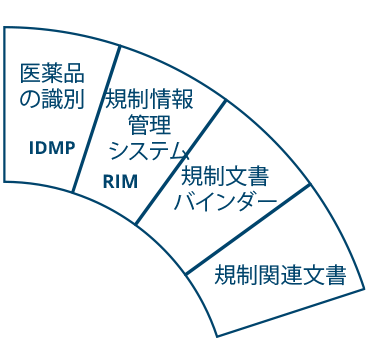
IDMP管理を合理化
ISO IDMP(Identification of Medicinal Products)規格は、医薬品に関する情報を識別・交換するためのデータ要素、フォーマット、用語に関する一連の共通のグローバル規格です。
新しいIDMP規格の導入と段階的な実施は、組織がこれまでよりも大幅に多くの規制データを取得・管理する必要があることを意味し、業界全体にとって大きな課題となっています。
効果的なデータ管理には多大な努力が必要で、時間とコストがかかります。Ennov IDMPと弊社のIDMPサービスは、新しい規格に移行しながら、お客様のIDMPデータを維持するプロセスを合理化します。
IDMPデータの品質確保
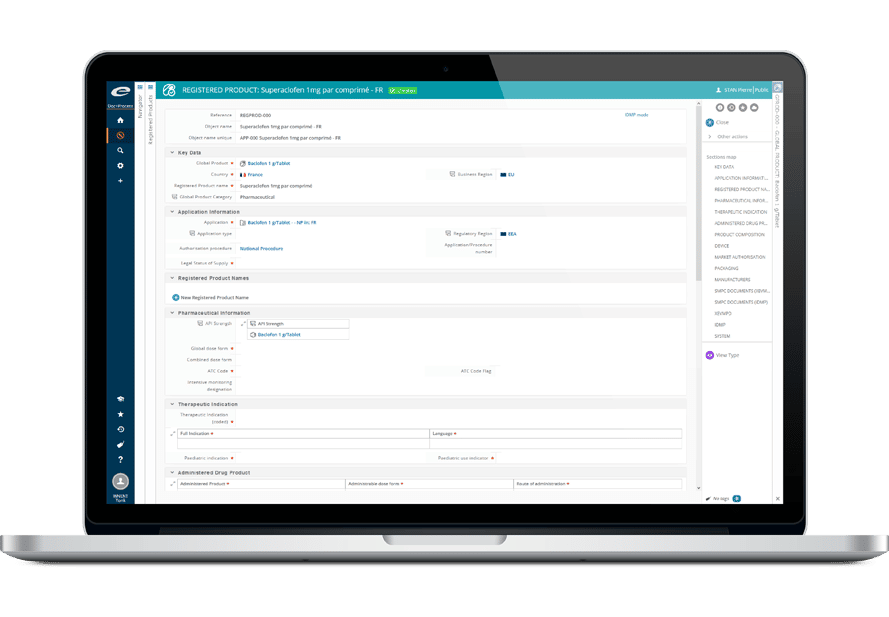
Ennov IDMPは、新規格のIDMPに対応したデータ管理のための品質管理ソリューションです。
既存のデータを活用して、IDMPへの取り組みを開始します。データのインベントリ、識別、クレンジング、統合を行い、組織をIDMPに対応させます。
規制文書やその他の企業システムに含まれる情報を取り出して抽出し、完全性を確保します。
未来へつなぐ
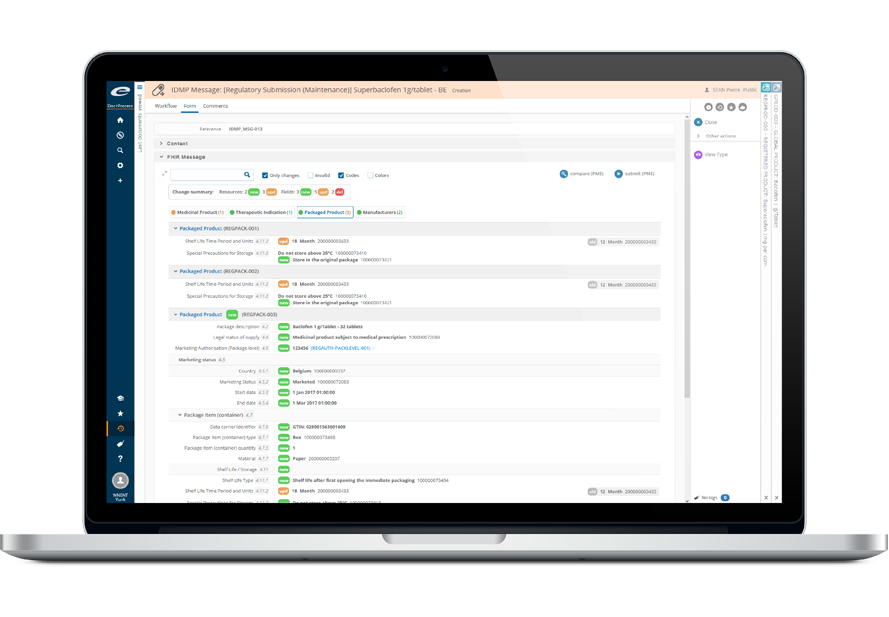
Ennov RIMはIDMPに対応しています。現在、システム内でEMA SPOR 参照文献リスト(統制語彙)をサポートしており、各データ要素に “IDMP用語”インジケータのフラグを立てています。
SPORデータサービスの仕様が進化すると、Ennov プラットフォームの柔軟性と構成可能性を最大限に活用して、体系的にソリューションに組み込みます。
Ennov IDMPは、包括的なRegulatory solution suiteの重要なコンポーネントです。Ennov Doc、Ennov RIM、Ennov Dossier、Ennov Report、そしてREST APIと組み合わせることで、Ennovは明日起こるかもしれないどんな問題にも対応できるソリューションを提供します。
IDMPコンプライアンスの準備
Ennovは、ISO IDMPの遵守が企業にとって大きな課題であることを認識しており、この課題への取り組みは規制リソースにさらなる負担をかけています。
Ennovは、業界がこの新しい基準の要件を効果的かつ効率的に満たすために、IDMP申請準備の重要な第一歩としてIDMP準備アセスメント・サービスを提供しています。
アセスメントを実施すると、様々なデータソース(構造化されたものとされていないものの両方)を特定し、IDMPに準拠するために取り組むべき欠落部を説明する文書化された評価が得られます。
中核となる機能
- 統制用語集が利用可能
- データの抽出、クレンジング、マイグレーションのサポート
- 実践的なIDMPデータ管理
- 時間と手間の節約
- データの品質と整合性の向上
主な特長
- メタデータ・オリエンテーション
- 高度な設定が可能
- 情報収集
- Ennov Regulatory Suiteとのシームレスな統合
- 優れたレポート作成と分析
Aguettantのケーススタディ
薬事規制システムマネージャ Cyrille JEUNE
Ennov Regulatory
世界最高水準の規制コンテンツと情報管理
Ennov Regulatory Suite は Ennov Doc、Ennov Dossier、Ennov Process の機能と柔軟性を組み合わせ、登録目標の初期計画から製品の廃止まで、規制当局の製品ライフサイクル全体にわたってサポートするものです。Ennov Regulatory Suiteは、規制当局の活動計画、製品登録管理、資料作成、資料管理などにおいて非常に有用なツールです。
Ennovを選ぶ理由
Ennovを信頼する数百社の顧客企業
20年以上にわたるライフサイエンス分野におけるソフトウェアソリューションの提供経験
ライフサイエンス分野の顧客は250社以上、その他の業界も多数
最新のアーキテクチャとインタフェース
WEBベース100%. 高い拡張性. ユーザー重視の設計
お客様の成功のために
顧客満足度が非常に高く、98.5%のプロジェクトが期限内、予算内に納品されている
お客様の選択の自由を尊重
クラウドベースまたはオンプレミスでの導入が可能
配置オプションの切り替えはいつでも可能
お客様の自主性を尊重
システム構成および管理に関するITスキルは不要
セキュリティの向上とパフォーマンスの最適化
データはローカルに保存されるが、柔軟性に富む。シングルテナントであるため、業務の中断を最小限に抑えられる

クラウドベースまたはオンプレミス

マルチプラットフォーム